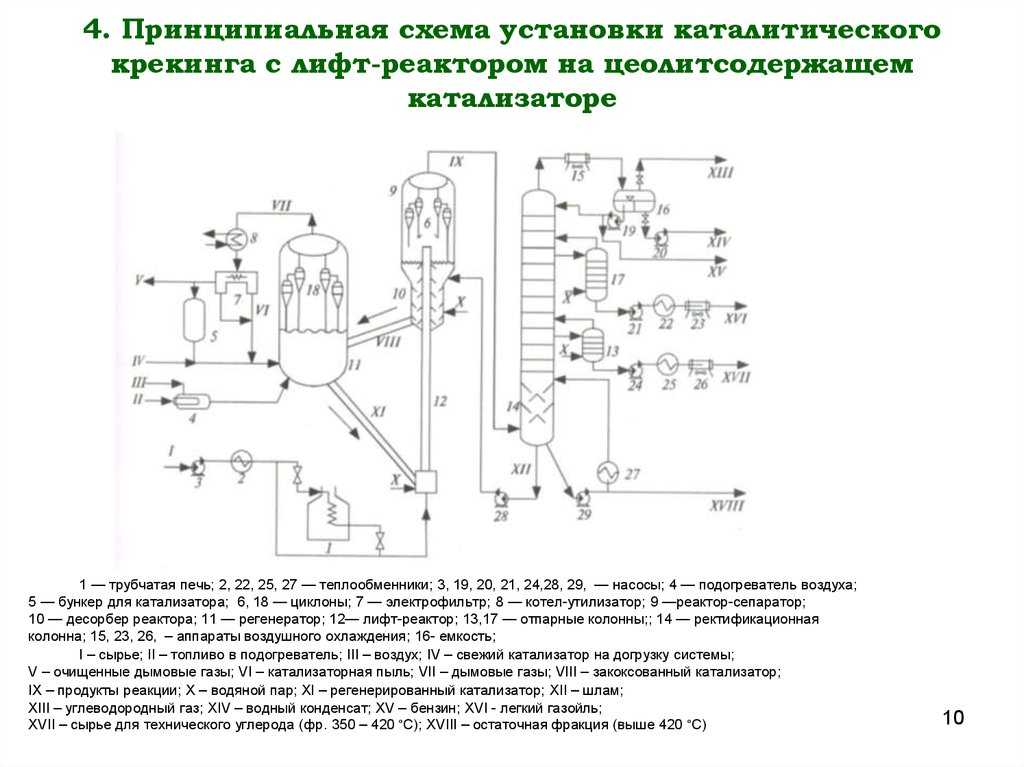
Требования к катализатору
Процесс FCC устанавливает ряд требований к параметрам катализатора:
- Активность, селективность и доступность: прежде всего, каталитические свойства для превращения крупных молекул исходного сырья в нужные молекулы;
- Стойкость к истиранию: частицы катализатора должны выдерживать удары друг о друга и стенки агрегата во время циркуляции;
- Гидротермическая стабильность: катализатор должен выдерживать температуру и парциальное давление пара в регенераторе;
- Толерантность к металлам: катализатор должен быть способен выдерживать действие ядов в (более тяжелом) исходном сырье;
- Селективность кокса: катализатор должен производить минимальное количество кокса при высокой активности крекинга, особенно при переработке более тяжелого сырья, такого как остатки;
- Флюидизируемость: компоненты катализатора должны быть доступны в форме, допускающей флюидизацию в регенераторе.
Принцип работы
В химии катализатор — это вещество, ускоряющее или вызывающее химическую реакцию, но само при этом не расходующееся. Такими веществами являются золото, никель, палладий, медь, родий, хром и большинство драгоценных и редких металлов.
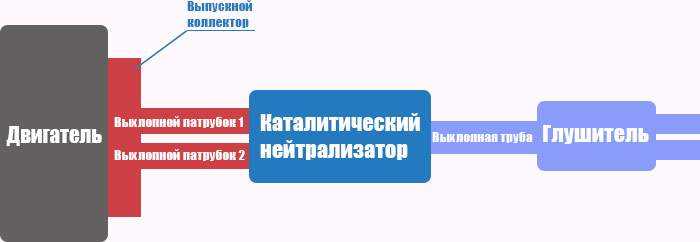
В процессе работы автомобильного двигателя образуются выхлопные газы. Эти газы попадают в выпускной коллектор и далее — в каталитический преобразователь.
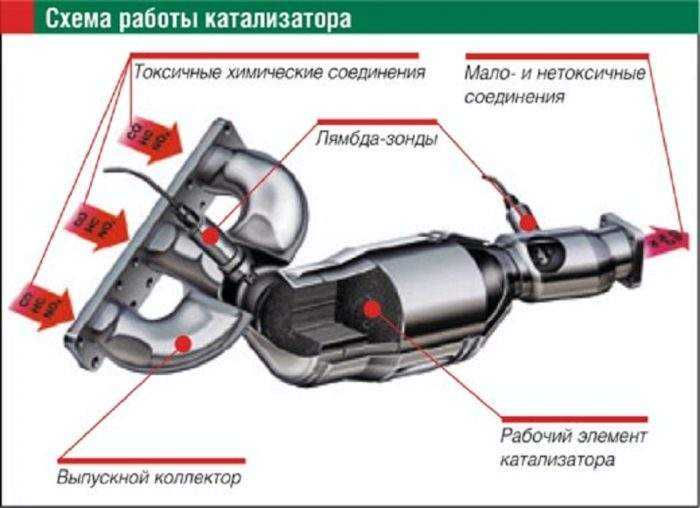
Выхлопной газ, состоящий из токсичных веществ, проходит через структуру нейтрализатора. Вещества-катализаторы в составе конвертера вызывают химические реакции, преобразующие вредные вещества в безвредные.
Современный нейтрализатор использует два катализатора, а именно — катализатор восстановления и катализатор окисления.
Катализатор окисления изготовлен из палладия и платины, а катализатор восстановления — из родия и платины. В результате реакций в каталитическом преобразователе образуются: углекислый газ, азот, вода.
Типы каталитических нейтрализаторов
Есть три разных типа автомобильных катализаторов. Первый тип — катализатор окисления. Он уменьшает вредные загрязнения, такие как угарный газ (CO) и углеводороды топлива (HC) в выхлопе. Одновременно часто используется вторичный впрыск воздуха. Однако катализатор окисления уменьшает только часть загрязняющих веществ.
Двухступенчатый катализатор
Второй тип — двуступенчатый каталитический нейтрализатор, который является более совершенным. Работает в два этапа. Есть два элемента, которые расположены один за другим.
Двусторонний (или «окислительный») каталитический нейтрализатор имеет две одновременные задачи:
- Окисление оксида углерода до диоксида углерода:2CO + O2 → 2CO2.
- Окисление углеводородов (несгоревшего и частично сгоревшего топлива) до диоксида углерода и воды:CxH2x + 2 + O2 → xCO2 + (x + 1) H2O (реакция горения).
Этот тип автомобильных катализаторов широко используется в дизельных двигателях для снижения выбросов углеводородов и окиси углерода. Они также использовались на бензиновых двигателях в автомобилях американского и канадского рынков до 1981 года. Из-за неспособности контролировать оксиды азота они были заменены трехступенчатыми нейтрализаторами.
Трёхступенчатый катализатор
Третий тип — это трёхступенчатый каталитический нейтрализатор. Начал использоваться с 1981 г. Он преобразовывает вредные газы, выходящие из двигателя, в безвредные.

Выхлопные газы двигателя содержат опасные вещества, которые наносят вред окружающей среде. К ним относятся оксиды азота, углеводороды и оксид углерода. Трехступенчатый катализатор превращает их в менее вредный диоксид углерода, воду и азот.
Три ступени очистки выхлопных газов выглядят так:
- Восстановление оксидов азота до азота (N2):2 CO + 2 NO → 2 CO2 + N2углеводород + NO → CO2 + H2O + N22 H2 + 2 NO → 2 H2O + N2;
- Окисление угарного газа до углекислого газа:2 CO + O2 → 2 CO2;
- Окисление несгоревших углеводородов (HC) до диоксида углерода и воды в дополнение к вышеуказанной реакции NO:углеводород + O2 → H2O + CO2;
Эти три реакции происходят наиболее эффективно, когда катализатор получает выхлоп от двигателя, работающего немного выше стехиометрической точки. Для сжигания бензина это соотношение составляет от 14,6 до 14,8 частей воздуха на одну часть топлива. Эффективность преобразования очень быстро падает, когда двигатель работает вне этих пределов.
При бедной смеси выхлоп содержит избыточный кислород и это не способствует реакции восстановления NOx. При богатой смеси избыточное топливо потребляет весь доступный кислород перед нейтрализатором, оставляя для функции окисления только кислород, находящейся в катализаторе.
Трёхступенчатый катализатор является единственным устройством, которое уменьшает количество всех трёх загрязнителей за один раз. Такой способ очистки наиболее экономичный.
Большинство автопроизводителей используют в своих транспортных средствах именно трехступенчатые нейтрализаторы, которые соответствуют строгим нормам выбросов.
Механизм крекинга
Наиболее вероятным механизмом каталитического крекинга углеводородов считается карбоний-ионный. Активация молекул углеводородов различного класса может проходить как на бренстедовских, так и на льюисовских кислотных центрах катализатора. Предполагают, что активация олефинов осуществляется на бренстедовских кислотных центрах, а парафины, циклопарафины и алкилароматические углеводороды могут активироваться на обоих типах кислотных центров.
Важную роль в каталитическом крекинге играет процесс перераспределения водорода, который в значительной степени формирует химический состав бензина каталитического крекинга (БКК) и, следовательно, определяет его октановое число. Существует мнение, что высокое содержание редкоземельных элементов в цеолитном катализаторе отрицательно влияет на октановые характеристики БКК.
Основные положения теории полифункционального катализа
Мо\нефункциональный катализатор — это катализатор, который содержит только один тип каталитически активных центров . Термин «один тип» означает, что все каталитически активные центры или участки поверхности ускоряют реакции одного типа или протекающие по одному и тому же механизму. Полифункциональный катализатор — это катализатор, который содержит два и более «типов» каталитически активных центров , каждый из которых ускоряет реакции, протекающие по отличающимся механизмам.
Очень важным в теории полифункционального гетерогенного катализа является также понятие «промежуточного соединения». Здесь не имеется в виду «активированные комплексы». Промежуточные соединение — это химическая частица, которая образуется под действием катализатора в виде десорбирующихся химических частиц, имеющих свое название, структуру и термодинамические свойства.
Промежуточное соединение может превращаться по разным маршрутам, что играет важную роль в последовательности монофункциональных каталитических реакций и влияет на скорость образования конечных продуктов.
Список литературы Катализаторы на основе цеолитов и цеолитоподобных материалов для переработки легкого углеводородного сырья в компоненты моторных топлив
- Капустин В.М. Основные направления модернизации и строительства нефтеперерабатывающих и нефтехимических комплексов в России//Материалы школы-конференции по нефтехимии. -Звенигород, 2009. -С. 61-62.
- Капустин В.М., Чернышова ЕА. Основные каталитические процессы переработки нефти. Промышленный катализ в лекциях. -М.: Калвис, 2006. -№ 5.
- Магарил Р.З. Теоретические основы химических процессов переработки нефти. -М.: Химия, 2008. -279 с.
- Шириязданов Р.Р., Рахимов М.Н., Мансуров И.С. Основные проблемы, особенности и перспективы переработки нефтезаводских газов//Нефтепереработка и нефтехимия. -2010. -№ 1. -С. 32-35.
- Галимов Ж.Ф., Рахимов М.Н. Силикафосфатные катализаторы олигомеризации нефтезаводских газов. Синтез, свойства и применение. -Уфа: Реактив, 1999.
- Khamzin Yu.A., Shiriyazdanov R.R., Davletshin A.R., Vildanov F.Sh., Ipatova E.A., Rakhimov M.N., Telyashev E.G., Abdyushev R.R., Doinitsyna L.S. Oligomerization of Propane-Propylene Fraction of Oil Refinery Gases on Pillared Clay Based Super-acidic Catalysts//Chemistry and Technology of Fuels and Oils. -2015. -V. 51. -№ 5. -pp. 458-463.
- Shiriyazdanov R.R., Davletshin A.R., Vildanov F.Sh., Telyashev E.G., Rakhimov M.N., Ipatova E.A., Abdyushev R.R., Khamzin Yu.A. Processing Refinery Gas Streams into Environmentally Friendly Motor Oils on Next-Generation Catalysts//Chemistry and Technology of Fuels and Oils. -2014. -V. 50. -№ 6. -pp. 465-471.
- Шириязданов Р.Р., Давлетшин А.Р., Рахимов М.Н., Хасанов Т.А., Гильмутдинов А.Т., Николаев Е.А. Олигомеризация олефинов С3-С4 на нанокомпозитном кислотно-активированном монтмориллоните, модифицированном ZrO2//Химическая промышленность сегодня. -2010. -№ 12. -С. 32-36.
- Лавренов А.В., Богданец Е.Н., Дуплякин В.К. Твердокислотное алкилирование изобутана бутиленами: путь от выяснения причин быстрой дезактивации катализаторов к технологическому оформлению процессов//Катализ в промышленности. -2009. -№ 1. -С. 28-38.
- Миначев Х.М., Мортиков Е.С., Зеньковский С.М., Мостовой Н.В., Кононов Н.Ф.//Алкилирование. Исследование и промышленное оформление процесса. -М.: Химия, 1982. -С. 81-86.
- Леонтьев А.С., Хаджиев С.Н., Зюба Б.И и др. Алкилирование изопарафинов олефинами на цеолитных катализаторах//Химия и технология топлив и масел. -1978. -№ 10. -С. 29-32.
- Цуприк Я.Е., Галич П.Н., Патриляк К.И. и др. Исследование влияния катионного состава цеолитов типа Y на их каталитические свойства в реакции алкилирования изобутана бутиленами//Нефтепереработка и нефтехимия. -1983. -№ 25. -С. 51-54.
- Зеньковский С.М., Мортиков Е.С., Погорелов А.Г. и др. Алкилирование изобутана н-бутаном на цеолитном катализаторе//Нефтехимия. -1975. -Т. 15, № 14. -С. 516-520.
- Миначев X.Н., Мортиков Е.С., Зеньковский С.М., Олбрайт Л.Ф., Голдсби А.Р. Алкилирование изопарафинов олефинами на цеолитных катализаторах. Алкилирование. Исследование и промышленное оформление процесса. -М.: Химия, 1982. -81-86 c.
- Мортиков Е.С., Зеньковский С.М., Мостовой К.Е. и др. Алкилирование изобутана бутиленами на цеолитных катализаторах//Химия и технология топлив и масел. -1974. -№ 7. -С. 13-16.
- Байбурский В.Л., Александрова И.А., Мортиков Е.С. Технология производства цеолитных катализаторов алкилирования изопарафиновых углеводородов//Нефтепереработка и нефтехимия. -1984. -№ 8. -С. 14-16.
- Байбурский В.Л., Александрова И.А., Хаджиева Л.X. и. др. Закономерности синтеза и свойства цеолитных катализаторов алкилирования изопарафиновых и ароматических углеводородов олефинами//Сб. науч. тр. ГрозНИИ. -1984. -№ 38. -С. 97-100.
- Коклин А.Е., Чан В.М.Х., Казанский В.Б., Богдан В.И. Алкилирование изобутана олефинами С4 в традиционных и сверхкритических условиях//Кинетика и катализ. -2010. -№ 3. -С. 429-434.
- Шириязданов Р.Р. Суперкислотные цеолитные каталитические системы для алкилирования изобутана олефинами//Ползуновский вестник. -2010. -№ 3. -С. 121-127.
- Шириязданов Р.Р. Наноструктурированные цеолитные катализаторы алкилирования изобутана бутан-бутиленовой фракцией//Нанотехника. -2010. -С. 59-60.
- Кудрявцев П.Г., Фиговский О.Л. Нанокомпозитные органоминеральные гибридные материалы//Нанотехнологии в строительстве. -2016. -№ 1. -С. 16-56.
- Грязнов И.В., Фиговский О.Л. Новая технология изготовления полимерных нанопорошков//Нанотехнологии в строительстве. -2015. -№ 6. -С. 28-57.
Бифункциональные цеолитные катализаторы
Схема 1. Схема тривиального бифункционального катализа
А — (X) — В — (Y) — С
X и Y соответственно типы реакционных центров.
Схема 2. Схема нетривиального бифункционального катализа
А м+ (X) «- В — (Y) — С
X и Y соответственно типы реакционных центров.
Если но втором случае выход продукта первой стадии лимитируется термодинамическим равновесием, то есть К = Кі/кг « 1, то при последовательном осуществлении данной схемы, суммарная степень превращения будет очень мала (кі и Кг — константы скоростей прямой и обратной реакций первой стадии).
Однако, если считать, что все стадии протекают по первому порядку, то щах =[А/(1/К + к3/К)) и может быть сколь угодно малой (к3 — константа скорости второй стадии), с другой стороны скорость суммарного превращения: dN/dt = К», а К» = кз/(1/К + KVKI) И значение К» можно сделать сколь угодно большим соответствующим подбором констант скоростей кі и ку, в этом случае возможно, что Єдс » ЄдвЄвс, где Є — это степени превращения на соответствующих стадиях.
Последнее соотношение и служит определением нетривиальной стадийной реакции, для тривиальной стадийной реакции Єдс = ЄАВЄВС
Влияние состава реакционной смеси на превращение модельной смеси №1 на Fe-содержащем цеолите HZSM-5
Ранее было показано, что на цеолите со структурой ZSM-5, в том числе с частичным изоморфным замещением в алюмокремнекислородном каркасе атомов алюминия на атомы железа , можно вести реакции синтеза из парафинсодержащего сырья высокооктановых компонентов моторных топлив — изо-парафиновых и ароматических углеводородов. В то же время известно, что активность и селективность действия цеолитов ZSM-5 зависит от природы атмосферы, в которой происходит превращение углеводородного сырья .
В результате проведенных исследований показано, что при превращении модельной углеводородной фракции как в атмосфере азота, так и в атмосфере водорода протекают первичные реакции разрыва С-С связи молекул исходных парафинов и вторичные реакции перераспределения водорода, приводящие к образованию легких парафинов С1-С4 и ароматических углеводородов Сб+. Основными расходуемыми веществами-реагентами исходного сырья являются н-гексан и циклогексан, а изооктан при низких и умеренных температурах процесса вследствие молекулярно-ситового эффекта на ZSM-5 не превращается , поэтому далее для первых и будут рассмотрены степени превращения.
Структура и состав катализатора
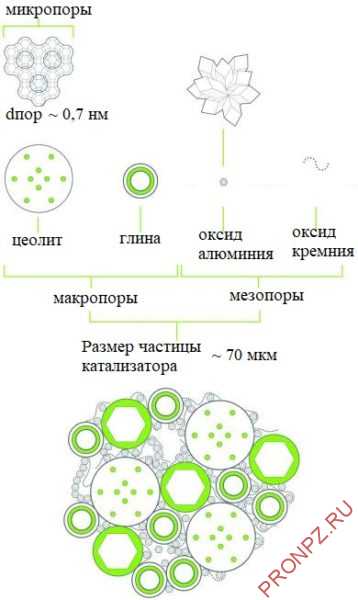 Типичный структурный и химический состав частицы микросферического катализатора
Типичный структурный и химический состав частицы микросферического катализатора
Основным активным компонентом является цеолит, обычно стабилизированная форма цеолита Y.
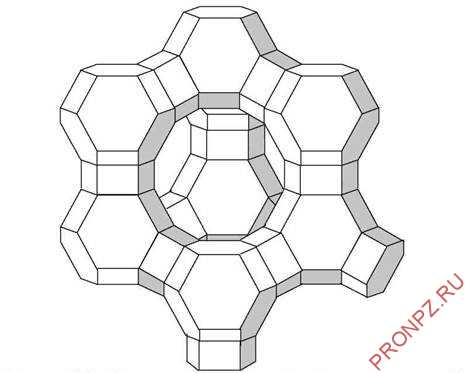 Структура элементарной ячейки цеолита типа Y
Структура элементарной ячейки цеолита типа Y
Этот материал содержит внутреннюю пористую структуру, в которой присутствуют кислотные участки, которые могут преобразовывать более крупные молекулы в молекулы желаемого бензинового диапазона. Глина добавляется в качестве наполнителя, но также и по причинам теплоемкости. Различные источники оксидов алюминия и кремния используются для получения мезо-и макропористой матрицы, которая позволяет прохождение более крупных молекул сырья и их предварительное крекирование. Кроме того, эти компоненты используются для связывания системы вместе. Дополнительные компоненты могут содержать специальные металлические ловушки для улавливания Ni и V. Компоненты обычно смешиваются в водной суспензии, а затем высушиваются распылением с образованием более или менее однородных сферических частиц, которые могут быть флюидизированы в регенераторе.
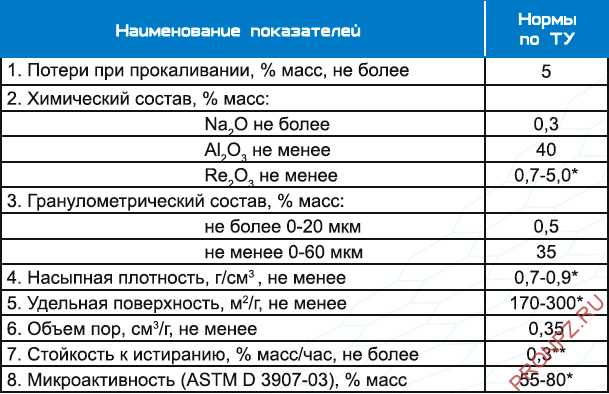 Типичный состав микросферического катализатора ОКТИФАЙН (KNT Group)
Типичный состав микросферического катализатора ОКТИФАЙН (KNT Group)
Формула изобретения
1. Цеолитсодержащий катализатор для получения моторных топлив из нефтяных дистиллятов и газовых конденсатов, содержащий цеолит группы пентасила с остаточным содержанием оксида натрия, связующий компонент и оксид металла, отличающийся тем, что он содержит цеолит ZSM-5 с силикатным модулем SiO2/Al2 O3=20-80 моль/моль и остаточным содержанием оксида натрия 0,02-0,05 мас.%, оксид висмута в качестве элемента структуры цеолитного компонента при следующем содержании компонентов, мас.%:
| цеолит ZSM-5 | 70,00-85,00 |
| Bi2 O3 | 1,0-6,00 |
| Na2 O | 0,02-0,05 |
| связующий компонент | остальное |
2. Способ получения цеолитсодержащего катализатора по п.1, включающий операции смешения реагентов, гидротермальный синтез, промывку, сушку и прокаливание осадка, при этом реакционную смесь, полученную путем смешения водных растворов солей алюминия, висмута, гидрооксида натрия, силикагеля и/или кислоты кремниевой водной, затравочных кристаллов цеолита со структурой ZSM-5 в Na или Н-форме, структуро-образователя, например, н-бутанола, загружают в автоклав, в котором проводят гидротермальный синтез при температуре 160-190°С в течение 10-30 ч при постоянном перемешивании, после завершения гидротермального синтеза пульпу Na-формы цеолита фильтруют, полученный осадок промывают хозяйственно-питьевой водой и направляют на проведение солевого ионного обмена путем его обработки водным раствором хлорида аммония при нагревании и перемешивании пульпы, полученную после солевого ионного обмена пульпу фильтруют, промывают хозяйственно-питьевой водой и затем промывают водой деминерализованной до остаточного содержания оксида натрия 0,02-0,05 мас.%, в пересчете на высушенный и прокаленный продукт, промытый осадок аммонийной формы цеолита направляют на операцию приготовления катализаторной массы путем смешения аммонийной формы цеолита с активным гидрооксидом алюминия, полученную катализаторную массу подвергают экструзии и гранулированию, гранулы сушат при температуре 100-110°С и прокаливают при 550-650°С, прокаленные гранулы цеолитсодержащего катализатора классифицируют, отделяют фракцию готового цеолитсодержащего катализатора, а фракцию гранул <2,5 мм измельчают до однородного порошка и возвращают на операцию приготовления катализаторной массы.
3. Способ получения моторных топлив, включающий нагревание и пропускание сырья через цеолитсодержащий катализатор, отличающийся тем, что в качестве сырья используют пары прямогонной бензиновой фракции нефти или пары газового конденсата, которые пропускают через стационарный слой цеолитсодержащего катализатора по п.1, нагретого до температуры 300-440°С, при нагрузке катализатора по сырью 2 ч-1.
Разработана новая высокоэффективная технология, позволяющая превращать воду и углекислый газ в жидкое топливо
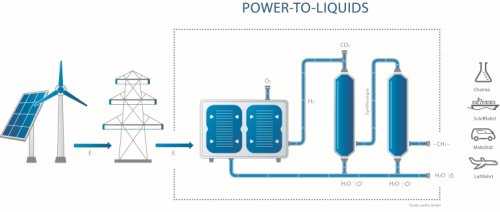
В настоящее время человечество во многом зависит от ископаемых видов топлива. Но, благодаря более широкому использованию энергии из альтернативных источников, энергии Солнца, энергии ветра, морских волн и т.п., эта зависимость начинает постепенно снижаться. Однако это очень тяжелый и болезненный процесс, ведь слишком много объектов промышленной и хозяйственной инфраструктуры завязаны на использовании угля, нефти, газа, и для их замены или модернизации требуется очень много времени, труда и денег. Временным выходом из этой ситуации может стать использование синтетического топлива, но, к сожалению, до последнего времени не было эффективной и экологически чистой технологии производства такого топлива. К счастью, эта ситуация недавно изменилась благодаря работе специалистов германской компании Sunfire GmbH.
Созданная компанией из Дрездена опытная установка, первая в своем роде реализация фирменной технологии под названием «Power-to-Liquid», позволяет преобразовать воду (H2O) и углекислый газ (CO2) в жидкие углеводороды, в синтетический бензин, керосин и дизельное топливо.
Основой технологии является так называемый процесс Фишера-Тропша (Fischer-Tropsch), разработанный еще в 1925 году, дополненный эффективной технологией твердо-оксидных электролизных ячеек (solid oxide electrolyser cells, SOEC). SOEC-ячейки используются для преобразования электрической энергии, поставляемой из возобновляемых источников, для расщепления воды на водород и кислород, который затем удаляется из состава нагретого до высокой температуры газа.

На следующем этапе процесса полученный водород реагирует с углекислым газом, извлеченным из атмосферы или получаемым в качестве побочного продукта в некоторых процессах производства химических веществ и пищевых продуктов. В результате этой реакции получается угарный газ (CO), который, снова реагируя с водородом, синтезирует углеводороды высокой степени чистоты при помощи процесса Фишера-Тропша. Излишки выделяющегося и остаточного тепла используются для повторного производства перегретого пара, что повышает уровень энергетической эффективности процесса в целом до 70 процентов.
В настоящее время компания Sunfire GmbH демонстрирует опытную установку, которая способна в сутки переработать до 3.2 тонн углекислого газа, произведя при этом баррель (159 литров) топлива. Стоимость исследований, проектирования и создания этой опытной установки выражается семизначным числом, большая часть которых была получена в рамках программы государственного финансирования от немецкого Федерального министерства образования и исследований (Federal Ministry of Education and Research).
«Наша опытная установка позволяет продемонстрировать возможность реализации разработанной нами технологии в промышленных масштабах» — рассказывает Кристиан фон Олсхаузен (Christian von Olshausen), один из руководителей компании Sunfire GmbH, — «Дальше все дело встанет лишь за привлечением инвесторов, которые понимают всю важность и долгосрочную перспективу избавления человечества от зависимости от ископаемых видов топлива». Источник
Источник
Стадии процесса каталитического крекинга
Процесс каталитического крекинга нефтяных фракций в кипящем слое микросферического цеолитсодержащего алюмосиликатного катализатора является одним из наиболее крупнотоннажных процессов нефтепереработки.
Постадийно процесс каталитического крекинга может быть представлен следующим образом:
- поступление сырья к поверхности катализатора;
- хемосорбция на активных центрах катализатора;
- химическая реакция на поверхности катализатора;
- десорбция продуктов крекинга и непрореагировавшей части сырья с поверхности и частично из внутренних пор катализатора;
- вывод продуктов крекинга из зоны реакции на последующую их ректификацию.
Подробное описание технологии каталитического крекинга представлено в статье.

Как превратить углекислый газ в полезную «химию»
Оксид индия вместе с медью неплохо справляется с восстановлением углекислого газа до угарного с помощью водорода.
Принципиальная схема обратной реакции конверсии водяного пара с химическим циклом (RWGS-CL). Илл.: Jun-Ichiro Makiura et.al., Chemical Science 2020.
Основной источник энергии для человечества сейчас – ископаемое топливо. Мы сжигаем уголь, природный газ и нефтепродукты, чтобы получить тепло или выработать электричество. Но при сжигании чего-то, содержащего углерод, обязательно образуется углекислый газ, а он, как известно, способствует такой нехорошей вещи, как глобальное потепление.
Поскольку отказаться здесь и сейчас от использования углеродного топлива мы пока по разным причинам не можем, то приходится делать хоть что-то, чтобы концентрация углекислого газа в атмосфере росла не так быстро. Поэтому разрабатываются технологии, превращающие углекислый газ во что-нибудь полезное, например, в сырьё для химического синтеза. Но что это значит с химической точки зрения?
В молекуле углекислого газа CO2 углерод прочно связан с двумя атомами кислорода. Чтобы от такого окисленного углерода была хоть какая-то химическая польза, от него нужно оторвать хотя бы один атом кислорода – превратить углекислый газ в газ угарный с формулой CO. Но для этого нужно затратить энергию, аналогичную той, которую мы бы получили, окислив угарный газ обратно до углекислого. Закон сохранения энергии, с которым всегда приходится считаться. Значит, для «чудесного» превращения углекислого газа в угарный нам нужен какой-то источник «чистой» энергии, которая не получена путём сжигания углеродного топлива. Предположим, что у нас он есть: какая-нибудь солнечная батарея или мощный ветрогенератор. Пусть даже мы с помощью «зелёного» электролиза получили из воды водород – газ, которым будем «химически» отрывать от углекислого газа один атом кислорода. Но и это ещё не всё.
Если взять углекислый газ, взять водород, смешать, погреть, потрясти и т.д., то мы, конечно, получим какое-то количество желанного нами угарного газа. Но, во-первых, его будет намного меньше, чем нам бы хотелось, а, во-вторых, это будет угарный газ вместе с исходными веществами и побочными продуктами реакции. Разделить полученную смесь можно, но на всё это потребуется затратить энергию, а её у нас и так дефицит. Чтобы выйти из этого затруднительного положения химики придумали метод, получивший название: обратная реакция конверсии водяного пара с химическим циклом (RWGS-CL).
Её суть состоит в том, чтобы разделить процесс отрыва атома кислорода от углекислого газа и его последующего «присоединения» к водороду на две отдельные стадии. Для этого необходимо использовать третье вещество, в роли которого обычно выступают оксиды металлов. В недавно опубликованной статье в журнале Chemical Science группа исследователей из университета Васэда и корпорации ENEOS предложила использовать для этой цели оксид индия, модифицированный медью. Как всё это работает?
На первой стадии углекислый газ вступает в реакцию с оксидом индия, который «отрывает» от CO2 один кислород и присваивает его себе. На выходе получается чистый угарный газ, без лишних примесей. Когда оксид индия насыщается кислородом, его регенерируют газообразным водородом, «вытаскивающим» лишний кислород из оксида, в результате чего получается обычная вода, а оксид индия возвращается в «боевое» состояние. Дальше цикл можно повторять. По утверждению авторов работы, главным достоинством такой системы с оксидом индия и медью служит её способность работать при более низких температурах, чем у известных аналогов.
Спасёт ли нас один лишь оксид индия на пару с медью от глобального потепления? По крайней мере, не в обозримом будущем. Даже если весь добываемый на планете металл индий (а это порядка одной тысячи тонн) пустить на борьбу с углекислым газом, то его вклад в понижение количества CO2 в атмосфере будет по приблизительным прикидкам на уровне одной тысячной от ежегодного объёма антропогенных выбросов CO2.
Однако не стоит называть подобные разработки бесполезными. Даже если отбросить такие экзотические, но всё же более-менее реальные задачи, как обеспечение жизнедеятельности колоний на Марсе или Луне, подобные технологии определяют направление возможных поисков решения и земных проблем тоже.
Источник
Катализатор дизельного двигателя
Для двигателей с воспламенением от сжатия (то есть для дизельных двигателей) наиболее часто используемым каталитическим нейтрализатором является катализатор окисления дизельного топлива (diesel oxidation catalyst — DOC).
DOC содержат палладий, платину и оксид алюминия, которые окисляют углеводороды и оксид углерода кислородом с образованием углекислого газа и воды.
- 2 CO + O2 → 2 CO2
- CxH2x + 2 + [(3x + 1) / 2] O2 → x CO2 + (x + 1) H2O
Эти преобразователи часто работают с 90-процентной эффективностью, фактически устраняя запах дизельного топлива и помогая уменьшить видимые частицы (сажу).
Эти конверторы не уменьшают NOx, потому что любой присутствующий восстановитель будет реагировать в первую очередь с высокой концентрацией O2 в выхлопных газах дизельного топлива.
Раньше сокращение выбросов NOx от дизельных двигателей решалось путем добавления выхлопных газов во впускной коллектор, известное как рециркуляция выхлопных газов (EGR).
В 2010 году большинство производителей дизелей добавили каталитические системы в свои автомобили, чтобы соответствовать новым требованиям по выбросам.
Дизельный выхлоп содержит высокий уровень твердых частиц (ТЧ). Каталитические нейтрализаторы не удаляют ТЧ, поэтому они очищаются сажевым фильтром (diesel particulate filter — DPF).
Все транспортные средства, работающие на дизельном топливе и изготовленные после 1 января 2007 года, должны соответствовать ограничениям на выбросы дизельных частиц, что означает, что они должны быть оснащены двухсторонним каталитическим преобразователем и иметь сажевый фильтр.
Предыдущая запись Датчик абсолютного давления (ДАД): как работает, неисправности, симптомы, как проверить
Следующая запись Катушка зажигания — виды, как работает, неисправности, как проверить
Где и как расположен катализатор
В большинстве транспортных средств каталитический нейтрализатор расположен рядом с выпускным коллектором двигателя. Преобразователь быстро нагревается благодаря воздействию очень горячих выхлопных газов, что позволяет снизить вредные выбросы во время прогрева двигателя.
Это достигается путем сжигания избыточных углеводородов, которые образуются в результате обогащенной смеси, необходимой для холодного пуска.
В некоторых трехкомпонентных катализаторах есть системы впрыска воздуха, который подается между первой (восстановление NOх) и второй (окисление углеводородов и СО) ступенью преобразователя.
Как и в двухступенчатых преобразователях, этот нагнетаемый воздух обеспечивает кислород для реакций окисления. Также иногда присутствует точка впрыска воздуха выше по потоку, перед каталитическим нейтрализатором, чтобы обеспечить дополнительный кислород только во время прогрева двигателя.
Это приводит к тому, что несгоревшее топливо воспламеняется в выхлопном тракте, тем самым предотвращая его попадание в каталитический конвертер. Этот метод сокращает время работы двигателя, необходимое для достижения рабочей температуры катализатора.
Датчики кислорода контролируют содержание кислорода в отработавших газах до и после каталитического нейтрализатора, и блок управления двигателем использует эту информацию для регулировки впрыска топлива.
Цеолитсодержащий катализатор
Цеолитсодержащие катализаторы ( цеолиты) характеризуются сочетанием высоких адсорбционных и каталитических свойств, большой избирательной способностью и стабильностью структуры, поэтому в настоящее время большое значение приобретают синтетические катализаторы с добавками цеолитов. При введении их, например, в состав алюмосиликатного катализатора крекинга значительно повышается его активность, избирательность, адсорбционная способность и паротермостабильность. Цеолиты могут быть получены как шариковые, так и микросферические.
Цеолитсодержащие катализаторы более стойки к отравлению металлами. На одной установке, работавшей на цеолитном катализаторе, при уменьшении количества догружаемого катализатора активность его заметно не понизилась, что свидетельствует о более высокой стойкости к отравлению металлами этого катализатора, чем обычного.
Цеолитсодержащие катализаторы при крекинге способствуют увеличению октанового числа бензина. Продукт, получаемый в результате такого крекинга, богат ароматическими углеводородами и парафинами с разветвленными цепями.
Цеолитсодержащие катализаторы проявляют меньшую восприимчивость к отравлению тяжелыми металлами, обычно присутствующими в сырье крекинга.
Цеолитсодержащие катализаторы, испытанные в процессе гидрокрекинга, проявляют активность при температурах, на 40 — 50 С ниже, чем аморфные; они обеспечивают выход бензина на 30 — 40 вес.
Цеолитсодержащий катализатор получен прямым синтезом.
Цеолитсодержащий катализатор очень чувствителен к отложениям кокса.
Цеолитсодержащие катализаторы отравляются азотом в про мышленных условиях в значительно меньшей степени, чем аморфные. Большая часть азота в сырье сосредоточена в высокомолекулярных полициклических ароматических углеводородах, и молеку-лярно-ситовые свойства цеолитов препятствуют отравлению их активных центров. Сернистые и кислородные соединения сырья на активность синтетических алюмосилякатных катализаторов не влияют.
Алюмоникельмояибдвновый цеолитсодержащий катализатор в условиях гидрокрекинга вакуумных дистиллятов обладает высокой расцепляющей и гидрирующей способностью. Скорость превращения углеводородов зависит как от оперативных условий процесса, так и содержания цеолита в катализаторе.
|
Результаты крекинга керосино-газойлевой фракции озексуатской нефти на различных катализаторах. |
Цеолитсодержащие катализаторы типа Y обладают высокой термической стабильностью. Присутствие редкоземельных металлов катализирует сгорание кокса. Установлено, что кокс на частицах начинает гореть при температуре на 100 — 110 С ниже, чем: температура начала горения кокса, отложившегося на матрице, поэтому вначале выгорает кокс с цеолитных участков. Последующее сгорание кокса с матричной основы может вызвать перегрев -, цеолитовых кристаллитов и нарушение их структуры. Поэтому вре -, мя регенерации таких катализаторов должно быть небольшим.
|
Зависимость октанового числа бензина от содержания катализатора Ок-такэт — П в смеси с CBZ-1. |
Современные зарубежные цеолитсодержащие катализаторы отличаются высокой активностью и селективностью, повыщен-ны-ми насыпной массой и износостойкостью.
Имеющийся цеолитсодержащий катализатор ГК-35 не следует считать лучшим для применения во всех вариантах процесса гидроочистки. По отдельным показателям, например в гидроочистке сырья реформинга, осуществляемого в жестком режиме на новых катализаторах, или в гидроочистке вакуумного газойля, он не достиг высших результатов и нуждается еще в усовершенствовании. Для промышленных испытаний предложены и новые катализаторы.
Цеолитсодержащему катализатору больше присущи реакции изомеризации, протекающие с выделением тепла, я в меньшей мере свойственные катализаторам старого типа. Кроме того, цеолитовые катализаторы значительно активнее и селективнее.