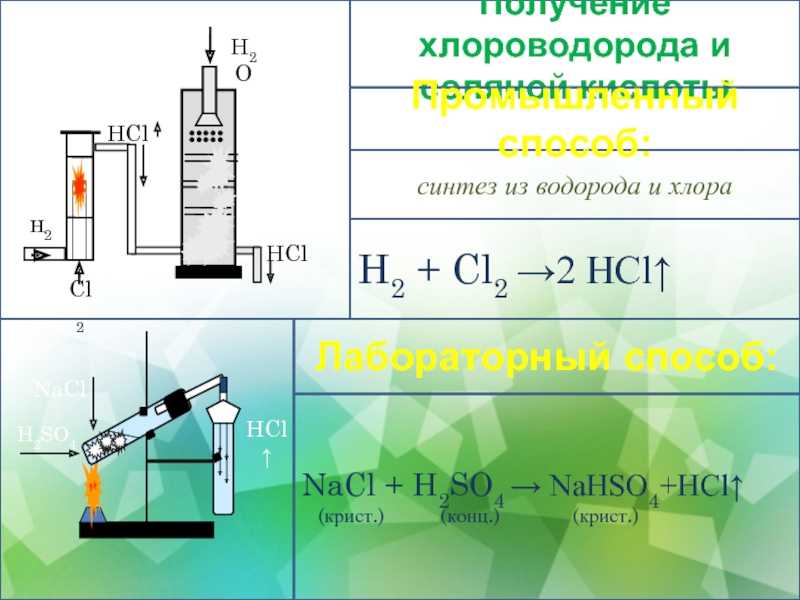
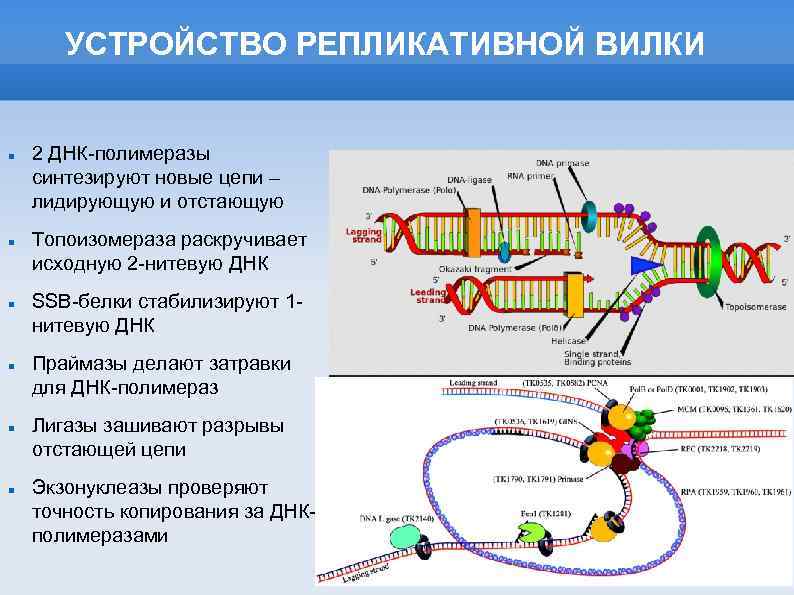
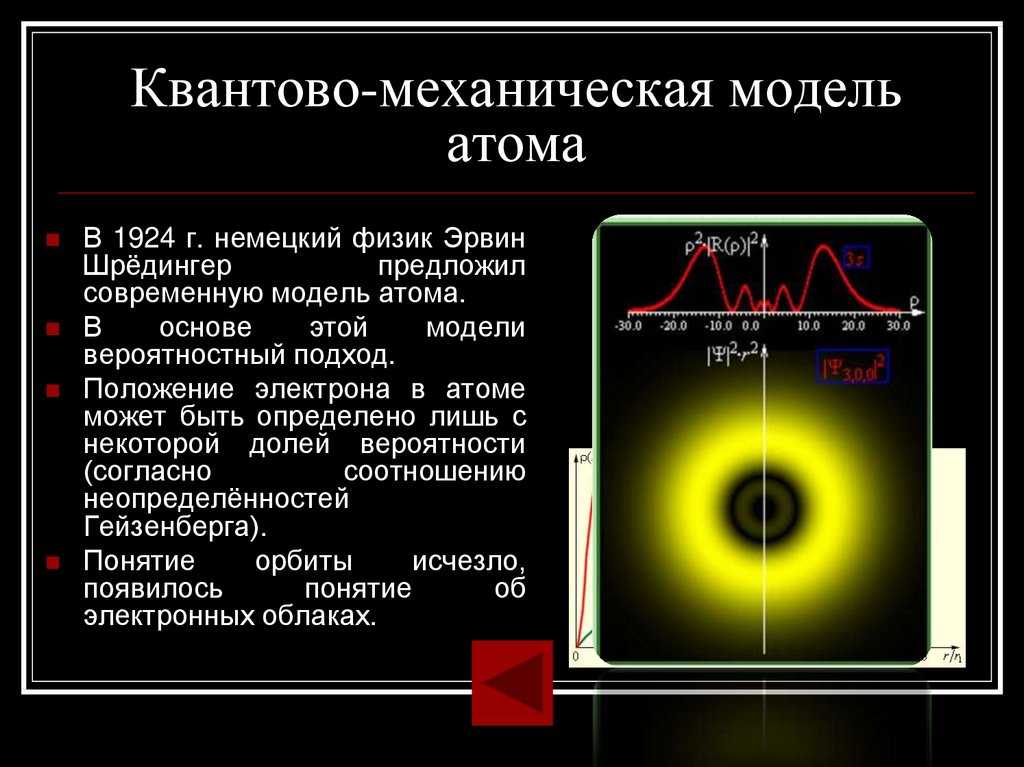
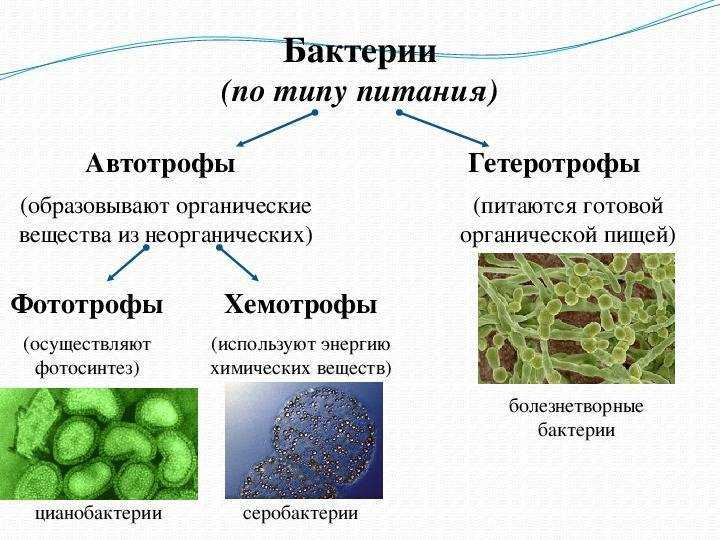
Области применения
Соляная кислота является важным и широко используемым химическим веществом.
В лабораториях соляная кислота применяется в качестве реагента в различных химических реакциях, а также при подготовке образцов для лабораторного анализа.
Наиболее часто соляная кислота используется при травлении стали, подкислении нефтяных скважин, производстве пищевых продуктов, производстве хлористого кальция и переработке руды.
Водный раствор соляной кислоты находит применение в самых разных областях промышленности и сферах деятельности человека.
К ним относятся извлечение полудрагоценных металлов из отработанных катализаторов, использование в качестве катализатора в синтезе веществ, использование в регенерации катализаторов, регулирование уровня рН, регенерация ионообменных смол, используемых в водоочистных сооружениях и электроэнергетике, нейтрализация щелочных продуктов или отходов, а также подкисление рассолов при производстве хлора и каустической соды.
Соляная кислота используется также во многих других промышленных производствах для получения органических химических веществ. Она может использоваться в производстве п-фенилендиамина, поликарбонатных смол, бисфенола А, поливинилхлоридных смол и этанола (из этилена).
В фармацевтической промышленности соляная кислота используется в качестве катализатора при синтезе веществ, для коррекции уровня рН, для деионизации воды и в качестве восстановителя (например, при производстве аскорбиновой кислоты и пара-аминобензойной кислоты).
Среди многих других областей применения соляной кислоты:
- Производство красителей и пигментов.
- Удаление шлама и накипи в промышленном оборудовании.
- Обеззоливание, дубление и покраска шкур в кожевенной промышленности.
- Производство лосьона для завивки волос.
- Карбонизация шерсти.
- Использование в качестве отбеливающего и красящего средства в текстильной промышленности.
- Очистка от песка и глины.
Примеры решения задач
| Задание | Какая масса оксида кремния (IV), содержащего 25% примесей,потребуется для получения силиката натрия массой 5,6 г по реакции с карбонатом натрия? |
| Решение | Запишем уравнение реакции взаимодействия оксида кремния (IV) с карбонатом натрия с образованием силиката натрия: |
Рассчитаем количество моль силиката натрия (молярная масса равна 122 г/моль):
Согласно уравнению реакции n (Na2SiO3) : n (SiO2) = 1: 1. Значит,
Тогда масса оксида кремния (IV) будет равна (молярная масса – 60 г/моль):
Учитывая наличие примесей в составе оксида кремния (IV) его масса будет равна:
m (SiO2) =3 × 0,25 = 0,75 г.
Ответ Масса оксида кремния (IV) равна 0,75 г.
| Задание | Какая масса кремниевой кислоты может быть получена при взаимодействии 500 мл 15%-ного раствора силиката натрия (плотность 1,1 г/мл) и соляной кислоты? |
| Решение | Запишем уравнение реакции: |
Найдем массу раствора силиката натрия, а также массу растворенного вещества Na2SiO3 в нем:
msolution =500 × 1,1 = 550 г.
Рассчитаем количество моль силиката натрия (молярная масса равна 122 г/моль):
n (Na2SiO3) = 82,5 / 122 = 0,676 моль.
Согласно уравнению реакции n (Na2SiO3) : n (H2SiO3) = 1: 1. Значит,
Тогда, масса образующейся кремниевой кислоты будет равна (молярная масса – 78 г/моль):
Источник
Применение
Более половины всего вырабатываемого пероксида водорода расходуется на отбелку
различных материалов, проводимую обычно в очень разбавленных (0,1-1%) водных
растворов Н2О2
Важное преимущество пероксида
водорода перед другими окислителями заключается в «мягкости»
действия, благодаря чему сам отбеливаемый материал почти не затрагивается. С
этим же связано и медицинское использование очень разбавленных раствором
пероксида водорода в качестве антисептика (для полоскания горла и т
д.).
Очень концентрированные (80% и выше) водные растворы Н2О2
находят применение в качестве источников энергии и самостоятельно (с помощью
катализаторов быстрого разложения Н2О2из одного литра жидкого пероксида водорода можно
получить около 5000 л нагретой до 700 °С смеси кислорода с водяным паром), и
как окислитель реактивных топлив. Пероксид водорода применяется как окислитель
в химических производствах, как исходное сырьё для получения пероксидных
соединений, инициатор полимеризационных процессов, при изготовлении некоторых
пористых изделий, для искусственного старения вин, крашения волос, вывода пятен
и т. д.
Применение соляной кислоты
Соляная кислота представляет собой одну из наиболее ценных кислот в химии. Ежегодно в мире производят миллионы тонн данного соединения. Соли соляной кислоты активно применяют в разных сферах хозяйственной деятельности. Краткий список областей использования соляной кислоты:
- гидрометаллургия;
- гальванопластика;
- травление, декапирование и лужение металлических поверхностей;
- пищевое производство (соляная кислота играет роль регулятора кислотности и является добавкой Е507);
- медицина (вещество в смеси с ферментом пепсином характеризуется лечебным эффектом и применяется в качестве лекарственного препарата при недостаточной кислотности желудка).
Желудок человека каждый день обновляет свою поверхность взамен пострадавшей от желудочного сока, в котором содержится соляная кислота. Соляная кислота обеспечивает переваривание пищи в желудке и устраняет разнообразные болезнетворные бактерии. Желудочный сок человека является достаточно агрессивным составом. К примеру, жидкость полностью растворяет бритвенное лезвие в течение недели. Данное свойство желудочного сока объясняется как раз наличием в составе соляной кислоты.
Получение водорода и его применение
Водород находит широкое применение в технике и лабораторных исследованиях. Мировое промышленное производство водорода из меряется десятками миллионов тонн в год.
Выбор промышленного способа получения простых веществ зависит от того, в какой форме соответствующий элемент находится в природе. Водород находится в природе преимущественно в соединениях с атомами других элементов. Поэтому для его получения необходимо использовать химические методы. Эти же методы применяют для получения водорода и в лабораторной практике.
Получение водорода в лаборатории
В лабораториях водород получают уже известным вам способом, действуя кислотами на металлы: железо, цинк и др. Поместим на дно пробирки три гранулы цинка и прильем небольшой объем соляной кислоты. Там, где кислота соприкасается с цинком (на поверхности гранул), появляются пузырьки бесцветного газа, которые быстро поднимаются к поверхности раствора:
Атомы цинка замещают атомы водорода в молекулах кислоты, в результате чего образуется простое вещество водород Н2, пузырьки которого выделяются из раствора. Для получения водорода таким способом можно использовать не только хлороводородную кислоту и цинк, но и некоторые другие кислоты и металлы.
Соберем водород методом вытеснения воздуха, располагая пробирку вверх дном (объясните почему), или методом вытеснения воды и проверим его на чистоту. Пробирку с собранным водородом наклоняем к пламени спиртовки. Глухой хлопок свидетельствует о том, что водород чистый; «лающий» громкий звук взрыва говорит о загрязненности его примесью воздуха.
Получение водорода в промышленности
Очевидно, что при огромных объемах промышленного производства сырьем для получения водорода должны быть легкодоступные и дешевые вещества. Такими веществами являются природный газ (метан СН4) и вода. Запасы природного газа очень велики, а воды — практически неограниченны.
Самый дешевый способ получения водорода — разложение метана при нагревании:
Эту реакцию проводят при температуре около 1000 °С.
В промышленности водород также получают, пропуская водяные пары над раскаленным углем:
Существуют и другие промышленные способы получения водорода.
Применение водорода
Водород находит широкое практическое применение. Основные области его промышленного использования показаны на рисунке 103.
Значительная часть водорода идет на переработку нефти. Около 25 % производимого водорода расходуется на синтез аммиака NH3. Это один из важнейших продуктов химической промышленности. Производство аммиака и азотных удобрений на его основе осуществляется в нашей стране на ОАО «Гродно Азот». Республика Беларусь поставляет азотные удобрения во многие страны мира.
https://youtube.com/watch?v=JTCzgKt9Kkg
В большом количестве водород расходуется на получение хлороводородной кислоты. Реакция горения водорода в кислороде используется в ракетных двигателях, выводящих в космос летательные аппараты. Водород применяют и для получения металлов из оксидов. Таким способом получают тугоплавкие металлы молибден и вольфрам.
В пищевой промышленности водород используют в производстве маргарина из растительных масел. Реакцию горения водорода в кислороде применяют для сварочных работ. Если использовать специальные горелки, то можно повысить температуру пламени до 4000 оС. При такой температуре проводят сварочные работы с самыми тугоплавкими материалами.
В настоящее время в ряде стран начаты исследования по замене невозобновляемых источников энергии (нефти, газа, угля) на водород. При сгорании водорода в кислороде образуется экологически чистый продукт — вода. А углекислый газ, вызывающий парниковый эффект (потепление окружающей среды), не выделяется.
Предполагают, что с середины XXI в. должно быть начато серийное производство автомобилей на водороде. Широкое применение найдут домашние топливные элементы, работа которых также основана на окислении водорода кислородом.
Профилактика
Чтобы снизить вероятность отравления HCL в бытовых или производственных условиях, требуется придерживаться следующих рекомендаций:
- Работать с токсичными веществами требуется в специальной одежде, защищающей весь кожный покров.
- Контактировать с HCL, эксплуатируя индивидуальные средства защиты, например, резиновые перчатки или респиратор.
- В помещении с концентрированным токсичным веществом требуется обеспечить хорошую вентиляцию.
- Кислоту требуется хранить правильно. Сама упаковка должна быть устойчива к воздействию хлористого водорода. На бутылку требуется нанести маркировку.
Получение вещества
Теперь можно поговорить о том, что делают для образования соляной кислоты.
Сначала, посредством сжигания в хлоре водорода, получают главный компонент — газообразный хлороводород. Который потом растворяют в воде. Результатом этой простой реакции становится образование синтетической кислоты.
Еще данное вещество можно получить из абгазов. Это — химические отходящие (побочные) газы. Они образуются при самых разных процессах. К примеру, при хлорировании углеводородов. Находящийся в их составе хлороводород называют абгазным. И кислоту, полученную таким образом, соответственно.
Следует отметить, что в последние годы доля абгазного вещества в общем объеме его производства увеличивается. А кислота, образованная вследствие сжигания в хлоре водорода, вытесняется. Однако справедливости ради нужно отметить, что в ней содержится меньше примесей.
![]()
Получение водорода в промышленности
В промышленности водород получают главным образом из природных и попутных газов, коксового газа и продуктов газификации топлива (водяного и паровоздушного газов), путем неполного окисления углеводородов.
Основным источником водорода в промышленности является конверсия (от лат. “превращение”) углеводородов, главным образом природного газа, парами воды (пароводяная конверсия):
CH4 + H2O → CO + 3H2, 800-900 °C, ΔH298 = 206,2 кДж/моль
С последующим каталитическим взаимодействием оксида углерода (II) с парами воды:
CO + H2O → CO2 + H2, 550-600 °C, ΔH298 = -41,2 кДж/моль
Катализатором этой реакции служит Fe2O3 с активирующими добавками (Cr2O3, Al2O3, K2O и др.).
Эндотермичность процесса конверсии метана можно частично восполнить энергией, выделяющейся при неполном его окислении.
2CH4 + O2 → 2CO + 4H2, ΔH298 = -71 кДж/моль
Этот процесс называется кислородной конверсией метана. Поэтому в промышленности часто комбинируют все эти три процесса в один. Для этого природный газ смешивается с водяным паром и кислородом:
3CH4 + O2 + H2O → 3CO + 7H2, 850-900 °C, Ni
или
2CH4 + O2 + 2H2O → 2CO2 + 6H2, 850-900 °C, Ni
Диоксид углерода удаляют промывкой газовой смеси водой под давлением и окончательно – поглощением растворами щелочей.
Все описанные выше процессы используются как по отдельности, так и в сочетании друг с другом.
Помимо природного газа для получения водорода путем конверсии используют генераторный (CO + N2), водяной (CO + H2) – пароводяная конверсия, попутные газы – пароводяная и (или) кислородная конверсия.
В связи с уменьшением запасов углеводородного сырья большой интерес приобретает метод получения водорода восстановлением водяного пара раскаленным углем:
C + H2O → CO + H2, 1000 °C, ΔH298 = 131 кДж/моль
При этом образуется генераторный газ. Затраты энергии на его получение можно компенсировать за счет реакции неполного окисления угля:
C + 1/2O2 → CO, ΔH298 = -110,5 кДж/моль
При комбинировании этих процессов получается водяной газ, состоящий в основном из смеси водорода и угарного газа:
3C + H2O + O2 → 3CO + H2
Важным следствием является то, что получаемые генераторный и водяной газы можно использовать для дальнейшего получения водорода методом пароводяной конверсии.
Из газовых смесей с большим содержанием водорода (коксовый газ, газы нефтепереработки) его получают путем глубокого охлаждения смеси, при котором практически все газы кроме водорода сжижаются.
Водород высокой чистоты получают электролизом водных растворов щелочей (NaOH или KOH). Раньше для этого использовалась серная кислота. Однако это нерационально из-за быстрого коррозионного разрушения стальной аппаратуры. Хотя образующаяся в процессе электролиза пероксодисерная кислота H2S2O8 может использоваться для получения пергидроля:
2SO42- – 2ê = S2O82-
H2S2O8 + H2O = H2SO5 + H2SO4
H2SO5 + H2O = H2SO4 + H2O2
В случае щелочей концентрация этих растворов выбирается такой, которая отвечает их максимальной электрической проводимости (25% для NaOH и 34% для KOH). Электроды обычно изготавливают из листового никеля. Этот металл не подвергается коррозии в растворах щелочей, даже будучи анодом. В случае надобности получающийся водород очищают от паров воды и следов кислорода. Этим способом целесообразно получать водород в районах с дешевой электроэнергией.
Водород образуется также как побочный продукт в процессе получения хлора и щелочей электролизом водных растворов хлоридов щелочных металлов.
Потенциальные способы получения водорода в промышленности
1. Термолиз воды:
2H2O → 2H2 + O2, 2000 °C, электрическая дуга.
Недостаток – большие расходы энергии.
2. Фотолиз воды:
2H2O → 2H2 + O2, hμ
3. Биохимическое разложение воды под действием бактерий.
4. Химическое разложение воды, восстановление водорода:
H2O + X = H2 + XO
2XO → 2X + O2, t°
Фосфор
Химический элемент фосфор расположен в 3-м периоде, V группе, главной подгруппе периодической системы Д.И. Менделеева. Его электронная формула 1s22s22p63s23p3.
Простое вещество фосфор существует в виде нескольких аллотропных модификаций (аллотропия состава). Белый фосфор Р4, при комнатной температуре мягкий, плавится, кипит без разложения. Красный фосфор Pn, состоит из полимерных молекул разной длины. При нагревании возгоняется. Чёрный фосфор состоит из непрерывных цепей Pn, имеет слоистую структуру, по внешнему виду похож на графит. Наиболее реакционноспособным является белый фосфор.
В промышленности фосфор получают прокаливанием фосфата кальция с углём и песком при 1500 °C:
![]()
В приведённые ниже реакции вступают любые модификации фосфора, если нет особых оговорок:
![]()
Фосфор образует летучее водородное соединение — фосфин, PH3. Это газообразное соединение с крайне неприятным резким запахом. Его соли в отличие от солей аммиака существуют только при низких температурах. Фосфин легко вступает в окислительно-восстановительные реакции:
![]()
Фосфор образует два кислотных оксида: P2O3 и P2O5. Последнему соответствует фосфорная (ортофосфорная) кислота H3PO4. Это трёхосновная кислота средней силы, которая образует три ряда солей: средние (фосфаты) и кислые (гидро- и дигидрофосфаты). Ниже приведены уравнения химических реакций, характерные для данных соединений:
![]()
Примечания и ссылки
- Уильям Л. Джолли, Современная неорганическая химия , McGraw-Hill, 1984, стр. 177
- рассчитывается молекулярная масса от .
- ↑ и
- Киран Ф. Лим , « Отрицательный pH действительно существует », Journal of Chemical Education , vol. 83,Октябрь 2006 г.
- ↑ and (en) Северин Остин и Арндт Гловацки, соляная кислота , Wiley-VCH Verlag, al. «Энциклопедия промышленной химии Ульмана»,15 июня 2000 г.
- (in) Гюнтер Зигемунд Вернер Швертфегер Эндрю Фейринг Брюс Смарт, Фред Бер, Хервард Фогель и Блейн МакКусик, Фторсодержащие соединения, органические соединения , Wiley-VCH Verlag, al. «Энциклопедия промышленной химии Ульмана»,15 июня 2000 г.
- ↑ и Справочник по экономике химических веществ , соляная кислота, SRI International, 2001, стр. 733 , 4000A-733.3003F
Физические свойства
Физические свойства соляной кислоты сильно зависят от концентрации растворённого хлороводорода:
| Конц. (вес),кг HCl/кг | Конц. (г/л),кг HCl/м³ | Плотность,кг/л | МолярностьM | Водородный показатель (pH) | Вязкость,мПа·с | Удельная теплоемкость,кДж/(кг·К) | Давление пара,Па | Температура кипения,°C | Температура плавления,°C |
| 10 % | 104,80 | 1,048 | 2,87 | −0,4578 | 1,16 | 3,47 | 0,527 | 103 | −18 |
| 20 % | 219,60 | 1,098 | 6,02 | −0,7796 | 1,37 | 2,99 | 27,3 | 108 | −59 |
| 30 % | 344,70 | 1,149 | 9,45 | −0,9754 | 1,70 | 2,60 | 1,410 | 90 | −52 |
| 32 % | 370,88 | 1,159 | 10,17 | −1,0073 | 1,80 | 2,55 | 3,130 | 84 | −43 |
| 34 % | 397,46 | 1,169 | 10,90 | −1,0374 | 1,90 | 2,50 | 6,733 | 71 | −36 |
| 36 % | 424,44 | 1,179 | 11,64 | −1,06595 | 1,99 | 2,46 | 14,100 | 61 | −30 |
| 38 % | 451,82 | 1,189 | 12,39 | −1,0931 | 2,10 | 2,43 | 28,000 | 48 | −26 |
При 20 °C, 1 атм (101 кПа)При затвердевании даёт кристаллогидраты составов HCl·H2O, HCl·2H2O, HCl·3H2O, HCl·6H2O.
Свойства
Водный раствор хлористого водорода называется соляной кислотой. При растворении в воде протекают следующие процессы:
Процесс растворения сильно экзотермичен. С водой HCl образует азеотропную смесь, содержащую 20,24 % HCl.
Соляная кислота является сильной одноосновной кислотой, она энергично взаимодействует со всеми металлами, стоящими в ряду напряжений левее водорода, с основными и амфотерными оксидами, основаниями и солями, образуя соли — хлориды:
Хлориды чрезвычайно распространены и имеют широчайшее применение (галит, сильвин). Большинство из них хорошо растворяется в воде и полностью диссоциирует на ионы. Слаборастворимыми являются хлорид свинца (PbCl2), хлорид серебра (AgCl), хлорид ртути(I) (Hg2Cl2, каломель) и хлорид меди(I) (CuCl).
При действии сильных окислителей или при электролизе хлороводород проявляет восстановительные свойства:
При нагревании хлороводород окисляется кислородом (катализатор — хлорид меди(II) CuCl2):
Однако, концентрированная соляная кислота реагирует с медью, при этом образуется комплекс одновалентной меди:
Смесь 3 объемных частей концентрированной соляной и 1 объемной доли концентрированной азотной кислот называется «царской водкой». Царская водка способна растворять даже золото и платину. Высокая окислительная активность царской водки обусловлена присутствием в ней хлористого нитрозила и хлора, находящихся в равновесии с исходными веществами:
Благодаря высокой концентрации хлорид-ионов в растворе металл связывается в хлоридный комплекс, что способствует его растворению:
Для хлороводорода также характерны реакции присоединения к кратным связям (электрофильное присоединение):
Какие вещества вступают в реакцию с соляной кислотой
На вступительных экзаменах по химии часто можно встретить задание на определение веществ, которые способны реагировать на соляную кислоту.
Кроме того, задание «составьте уравнение» нередко вызывает страх в глазах выпускников.
Чтобы не путаться с химическими задачами, рекомендуется подробнее изучить информацию о взаимодействии с данным соединением.
Все существующие вещества можно поделить на металлы, вытесняющие водород из соединения, не вытесняющие водород, а также активные и неактивные металлы.
В реакцию с соляной кислотой вступают такие вещества:
-
Химические основания. Соляная кислота способна нейтрализовать основания. Как известно, они состоят из атома металла, на который и воздействует кислота.
К ним относят гидроксид натрия, бария, алюминия. Реакция нейтрализации дает образования соли и воды. -
Металлы. Если обратиться к электрохимическому ряду, можно увидеть, что соляная кислота реагирует со всеми элементами, стоящими до водорода в этом ряду.
Сюда относят натрий, магний, алюминий, литий, барий, кальций, цинк, железо и другие элементы. При взаимодействии они образуют хлориды и выделяют газообразный водород. - Основные и атмосферные оксиды. Во время реакции происходит образование растворимых солей и воды. HCl взаимодействует с оксидом алюминия, меди, цинка, натрия.
-
Карбонаты. При взаимодействии с карбонатами кальция получится следующее уравнение: CaCO₃ + 2HCl→ CaCl₂ + CO₂↑ + H₂O.
Из него следует, что выделяется углекислый газ, а также образуется вода и угольная кислота. - Сильные окислители. Если вещество взаимодействует с перманганатом калия или диоксидом марганца, на выходе получается выделение газообразного хлора.
- Аммиак. Такое взаимодействие ознаменовано выделением сильного дыма, поэтому в момент проведения опытов рекомендуется открыть все окна. Тогда выделяется хлорид аммония.
Кроме перечисленных веществ и соединений, HCl также способна реагировать на нитрат серебра – при таком взаимодействии образуется осадок белого цвета творожистого типа.
Физические свойства
Чистый пероксид водорода — бесцветная
сиропообразная жидкость (с плотностью около 1,5 г/мл), под достаточно
уменьшенным давлением перегоняющуюся без разложения. Замерзание Н2О2
сопровождается сжатием (в отличие от воды). Белые кристаллы пероксида водорода
плавятся при -0,5 °С, т. е. почти при той же температуре, что и лёд.
Теплота плавления пероксида
водорода составляет 13 кДж/моль, теплота испарения — 50 кДж/моль (при 25 °С).
Под обычным давлением чистый Н2О2 кипит при
152 °С с сильным разложением (причём пары могут быть взрывоопасны). Для его
критических температуры и давления теоретически рассчитаны значения 458 °С и
214 атм. Плотность чистого Н2О2 равна 1,71
г/см3 в твёрдом состоянии, 1,47 г/см3 при 0 °С и 1,44 г/см3 при 25 °С. Жидкий
пероксид водорода, подобно воде, сильно ассоциирована. Показатель
преломления Н2О2 (1,41), а также её вязкость
и поверхностное натяжение несколько выше, чем у воды (при той же температуре).
Физические свойства [ править | править код ]
Физические свойства соляной кислоты сильно зависят от концентрации растворённого хлороводорода:
| Конц. (вес) , мас. % | Конц. (г/л) , кг HCl/м³ | Плотность , кг/л | Молярность , M | Водородный показатель (pH) | Вязкость , мПа·с | Удельная теплоемкость , кДж/(кг·К) | Давление пара , Па | Т. кип. , °C | Т. пл. , °C |
| 10 % | 104,80 | 1,048 | 2,87 | −0,4578 | 1,16 | 3,47 | 0,527 | 103 | −18 |
| 20 % | 219,60 | 1,098 | 6,02 | −0,7796 | 1,37 | 2,99 | 27,3 | 108 | −59 |
| 30 % | 344,70 | 1,149 | 9,45 | −0,9754 | 1,70 | 2,60 | 1,410 | 90 | −52 |
| 32 % | 370,88 | 1,159 | 10,17 | −1,0073 | 1,80 | 2,55 | 3,130 | 84 | −43 |
| 34 % | 397,46 | 1,169 | 10,90 | −1,0374 | 1,90 | 2,50 | 6,733 | 71 | −36 |
| 36 % | 424,44 | 1,179 | 11,64 | −1,06595 | 1,99 | 2,46 | 14,100 | 61 | −30 |
| 38 % | 451,82 | 1,189 | 12,39 | −1,0931 | 2,10 | 2,43 | 28,000 | 48 | −26 |
При 20 °C, 1 атм (101 кПа)
При низкой температуре хлороводород с водой даёт кристаллогидраты составов HCl·H2O (т. пл. –15,4 °С), HCl·2H2O (т. пл. –18 °С), HCl·3H2O (т. пл. –25 °С), HCl·6H2O (т. пл. –70 °С). При атмосферном давлении (101,3 кПа) хлороводород с водой образуют азеотропную смесь с т. кип. 108,6 °С и содержанием HCl 20,4 мас. % .
Свойства
Водный раствор хлористого водорода называется соляной кислотой. При растворении в воде протекают следующие процессы:
Процесс растворения сильно экзотермичен. С водой HCl образует азеотропную смесь, содержащую 20,24 % HCl.
Соляная кислота является сильной одноосновной кислотой, она энергично взаимодействует со всеми металлами, стоящими в ряду напряжений левее водорода, с основными и амфотерными оксидами, основаниями и солями, образуя соли — хлориды:
Хлориды чрезвычайно распространены в природе и имеют широчайшее применение (галит, сильвин). Большинство из них хорошо растворяется в воде и полностью диссоциируют на ионы. Слаборастворимыми являются хлорид свинца(II) (PbCl2), хлорид серебра (AgCl), хлорид ртути(I) (Hg2Cl2, каломель) и хлорид меди(I) (CuCl).
При действии сильных окислителей или при электролизе хлороводород проявляет восстановительные свойства:
При нагревании хлороводород окисляется кислородом (катализатор — хлорид меди(II) CuCl2):
Концентрированная соляная кислота реагирует с медью, при этом образуется комплекс одновалентной меди:
Смесь 3 объемных частей концентрированной соляной и 1 объемной доли концентрированной азотной кислот называется «царской водкой». Царская водка способна растворять даже золото и платину. Высокая окислительная активность царской водки обусловлена присутствием в ней хлористого нитрозила и хлора, находящихся в равновесии с исходными веществами:
Благодаря высокой концентрации хлорид-ионов в растворе металл связывается в хлоридный комплекс, что способствует его растворению:
Присоединяется к серному ангидриду, образуя хлорсульфоновую кислоту HSO3Cl:
Для хлороводорода также характерны реакции присоединения к кратным связям (электрофильное присоединение):
Это интересно: Водород фтористый (Фтороводород)
Соляная кислота
![]()
Главная / Лекции 1 курс / Общая и органическая химия / Вопрос 49. Хлороводород и соляная кислота / 2. Соляная кислота
https://youtube.com/watch?v=u9vs1N3sBYY
Раствор хлороводорода в воде называется соляной кислотой. Это сильная кислота, она реагирует со всеми металлами, стоящими в ряду напряжений левее водорода, с основными и амфотерными оксидами, основаниями и солями:
СuО + 2 НСl = СuСl2 + Н2О;
ZnO + 2 НСl = ZnСl2 + Н2О;
Fе(ОН)3 + 3 НСl = FеСl3 + 3 H2О;
АgNО3 + НСl = AgCl↓ + НNО3;
Кроме свойств, присущих сильным кислотам, эта кислота характеризуется также восстановительными свойствами: концентрированная соляная кислота реагирует с сильными различными окислителями с образованием свободного хлора.
Соли соляной кислоты называются хлоридами. Большинство из них хорошо растворяется в воде и полностью диссоциирует на ионы. Слаборастворимыми являются хлорид свинца (РbСl2), хлорид серебра (AgCl), хлорид ртути (I) (Нg2Сl2 каломель) и хлорид мели (I) (СuСl).
В такой башне свежие порции воды в верхней части башни встречаются с газовым потоком, содержащим уже мало хлороводорода, а газ с высоким содержанием хлороводорода в нижней части башни встречается с концентрированной соляной кислотой.
Так как растворимость газа в жидкости прямо пропорциональна концентрации его в газовой фазе и обратно пропорциональна концентрации его в растворе, при этом методе достигается полное извлечение хлороводорода из газа и получение концентрированного раствора соляной кислоты.
Насыщенный при комнатной температуре водный раствор хлороводорода может содержать не более 42 % масс хлороводорода и его плотность не превышает 1,20 г/см3. Поступающая в продажу соляная кислота содержит 36-37 % хлороводорода и имеет плотность 1,19 г/см3.
Важно
Соляную кислоту хранят и транспортируют в стальных цистернах, покрытых изнутри кислотоупорной резиной, или в стеклянных баллонах.
Хлороводород, соляную кислоту и ее соли широко используют в промышленности и лабораторной практике. Хлороводород применяют в органическом синтезе для получения хлорорганических соединений. Соляную кислоту используют для получения солей, травления металлов, а также как реактив в химических лабораториях.
Из солей соляной кислоты наибольшее применение находит:
- каменная, или поваренная, соль (NаСl). Она используется как сырье для получения хлора, металлического натрия, едкого натра, хлороводорода и соды, а также в пищевой промышленности;
- хлорид калия (КСl). Применяется как калийное удобрение, а также как сырье для получения других солей калия и едкого калия;
- хлорид кальция (СаСl2). Безводная соль применяется для высушивания газов и многих органических жидкостей и как осушительный агент в эксикаторах. При этом образуется кристаллогидрат СuСl2 * nН2О (n = 2-6). Насыщенный водный раствор хлорида кальция используют для обогащения сырья флотационным методом;
- хлорид бария (ВаСl2). Применяется как ядохимикат в сельском хозяйстве;
- хлорид цинка (ZnCl2). Используется при пайке для снятия пленки оксидов (травление металла), а также для пропитки деревянных предметов с целью предохранения их от гниения при закапывании в землю.
Далее по теме:
Библиография
- Справочник по экономике химических веществ, соляная кислота , SRI International, 2001.4000A-733.3003F.
- Ван Дорст, WCA и др. , Техническая брошюра по продукту «Соляная кислота» , AkzoNobel Base Chemicals, 2004 г.
- Ван Дорст, WCA, Различные технические документы , AkzoNobel Base Chemicals, 1996-2002 гг.
- Лиде, Дэвид, NIST, Справочник CRC по химии и физике , CRC Press, 61- е изд. , 1980–1981.
- Aspen Technology, Aspen Properties , программное обеспечение для моделирования бинарных смесей, расчеты AkzoNobel Engineering, 2002-2003 гг.
- Эвисон Д., Хинсли Д., Райс П., Химическое оружие , 2002, 324 (7333): 332-5, .
- Артур С. Гайтон, доктор медицины, Учебник медицинской физиологии Джона Э. Холла , WB Saunders Company, 10- е изд. ,15 августа 2000 г.( ISBN 978-0-7216-8677-6 ) .